自強課程

課程名稱
【勞動部勞動力發展署補助80%課程】醫療器材產品實現之設計管制要求與流程確效實務班第01期
熱烈招生中
[報名須上職訓局人才投資網站代碼 171431]。補助及報名詳情如下【注意事項】
1.了解醫療器材產品實現全生命週期之法規架構
2.了解國際法規對產品設計、製造與上市後管理的核心規範
3.理解醫療器材製程確效之法規與品質要求
4.透過案例研討與文件撰寫,強化實務應用能力
2.了解國際法規對產品設計、製造與上市後管理的核心規範
3.理解醫療器材製程確效之法規與品質要求
4.透過案例研討與文件撰寫,強化實務應用能力
課程代碼:
15B326
上課時間:
2026/12/05~12/19,每星期六,共三週,09:00~12:00;13:00~16:00
上課時數:
18 小時
課程費用:
3510元
(符合超值優惠價格者需送出報名表後,系統發出報名成功回函確認金額。)
課程目標:
本課程將指導學員如何規劃並執行製程確效,確保生產程序能持續穩定地產出符合標準之產品。最終,透過案例研討與文件撰寫實務,學員將能建立醫療器材產品技術文件,學會如何應對官方稽查中的各項技術細節,進而協助企業優化品質管理系統並降低產品開發與生產過程中的失效風險。
課程特色:
1.建立符合國際法規標準的醫療器材產品實現全週期知識體系
2.掌握 ISO 13485、美國 FDA 與歐盟醫療器材法規中之設計管制與品質系統要求
3.建立設計輸出、設計審查、設計驗證與設計確效之完整流程
4.建立可支援量產與查廠的製造品質文件
5.提升面對查廠、審查與法規溝通之專業應對能力
6.提升企業醫療器材產品上市與量產的成功率
2.掌握 ISO 13485、美國 FDA 與歐盟醫療器材法規中之設計管制與品質系統要求
3.建立設計輸出、設計審查、設計驗證與設計確效之完整流程
4.建立可支援量產與查廠的製造品質文件
5.提升面對查廠、審查與法規溝通之專業應對能力
6.提升企業醫療器材產品上市與量產的成功率
修課條件:
1.醫療器材在職人員訓練。
2.有意提升醫療器材產業與法規知識者。
3.從事電子、材料、設備、製藥、生技產業及臨床醫學之異業想投入醫療器材產業者。
2.有意提升醫療器材產業與法規知識者。
3.從事電子、材料、設備、製藥、生技產業及臨床醫學之異業想投入醫療器材產業者。
課程大綱:
1.產品適用之標準及法規評估策略:探討全球醫療器材法規環境的最新變革、評估產品適用的法規標準
2.醫療器材設計開發管制概念:解析從概念到產品實現的設計開發流程
3.醫療器材產品技術文件準備:建立與撰寫醫療器材產品技術文件的方法
4.設計開發的風險管理要求:導入風險管理思維於設計開發流程中
5.醫療器材產品實現之流程確效:深入解析量產階段的確效實務
6.醫療器材上市後監督與變更管制概念:說明產品上市後如何持續監控產品安全與效能及如何啟動變更管制流程
2.醫療器材設計開發管制概念:解析從概念到產品實現的設計開發流程
3.醫療器材產品技術文件準備:建立與撰寫醫療器材產品技術文件的方法
4.設計開發的風險管理要求:導入風險管理思維於設計開發流程中
5.醫療器材產品實現之流程確效:深入解析量產階段的確效實務
6.醫療器材上市後監督與變更管制概念:說明產品上市後如何持續監控產品安全與效能及如何啟動變更管制流程
課程師資:
自強專業講師
曾任職致慧顧問有限公司 醫療器材專案經理
福寶科技 產品工程師
工業技術研究院 工程師
曾任職致慧顧問有限公司 醫療器材專案經理
福寶科技 產品工程師
工業技術研究院 工程師
主辦單位:
勞動部勞動力發展署桃竹苗分署
執行單位:
財團法人自強工業科學基金會
學員須知:
注意事項
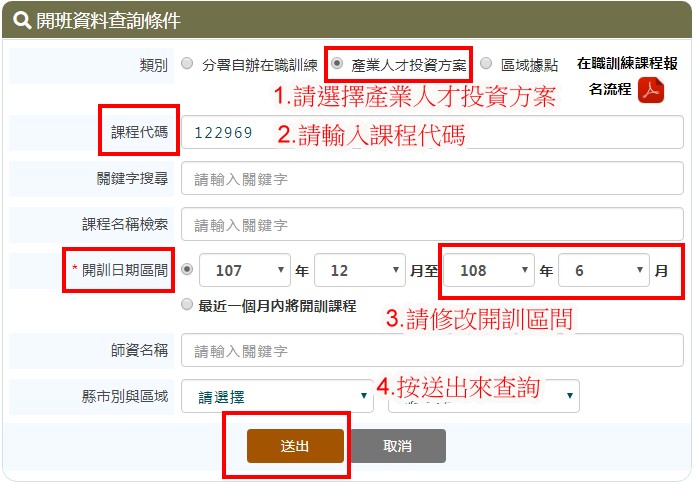
一、課程詳情請點「在職訓練網」,進入後點選「課程查詢報名」、「課程查詢」,再依下列四步驟查詢(請留意:課程代碼為171431),即可進入該課程介面。
二、自108年起新增「即時比對課程報名時段重疊」功能,民眾報名時,如與已報名或參訓中的課程有時段重疊情形,只能擇一參訓(與已報名課程重疊,應取消已報名課程,才能完成新課程報名;與參訓中課程重疊,即不得報名)。敬請於課程報名前,留意欲報名課程是否與其他已報名及參訓中之課程有時段重疊情形,以有效利用訓練資源。
三、其他事項提醒:
(一)報名「產業人才投資方案」課程時,應具備台灣就業通會員資格,若無台灣就業通會員資格的民眾,請先至台灣就業通網加入會員。
(二)參訓前請務必閱讀產業人才投資方案參訓學員須知說明若遇不可預測之突發因素,基金會保有相關課程調整、取消及講師之變動權。
無紙化環境,輕鬆達到減碳救地球,即日起16小時以上課程結業證書或未達16小時課程上課證明皆以電子方式提供。
本課程不適用廠商VIP折扣優惠
課前請詳閱簡章之課程內容或利用課程諮詢電話。
課程嚴禁旁聽,亦不可攜眷參與。
優惠方案擇一使用。

二、自108年起新增「即時比對課程報名時段重疊」功能,民眾報名時,如與已報名或參訓中的課程有時段重疊情形,只能擇一參訓(與已報名課程重疊,應取消已報名課程,才能完成新課程報名;與參訓中課程重疊,即不得報名)。敬請於課程報名前,留意欲報名課程是否與其他已報名及參訓中之課程有時段重疊情形,以有效利用訓練資源。
三、其他事項提醒:
(一)報名「產業人才投資方案」課程時,應具備台灣就業通會員資格,若無台灣就業通會員資格的民眾,請先至台灣就業通網加入會員。
(二)參訓前請務必閱讀產業人才投資方案參訓學員須知說明



